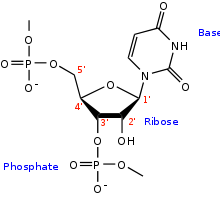
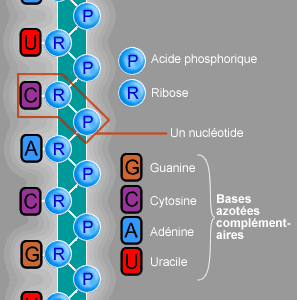
ARN et ADN (cf. ADN) ont des structures chimiquement proches. Ce sont des polymères linéaires constitués d’un enchaînement de nucléotides, c’est-à-dire de bases azotées, avec un groupement phosphate et un sucre (respectivement ribose et désoxyribose), et liés entre eux par une liaison phosphodiester. La thymine de l’ADN est remplacée par un uracile dans l’ARN, et la substitution du désoxyribose par un ribose rend l’ARN chimiquement moins stable que l’ADN.
L’ARN est généralement sous forme de simple brin dans la cellule (sauf chez quelques virus) et il est nettement plus court que l’ADN du génome (de quelques dizaines à quelques milliers de nucléotides pour le premier, de quelques milliers à quelques milliards pour le second). L’ARN est une copie d’une région de l’un des brins de l’ADN, une transcription réalisée par les ARN polymérases. Ce n’est qu’en 2001 que l’équipe de Harry Noller résolut la structure du ribosome entier, progrès essentiel dans la compréhension du mécanisme central du vivant qu’est la transcription.
L’ARN, support de l’information d’un ou plusieurs gènes codant des protéines est l’ARN messager. L’ARN peut, selon sa conformation, agir en système catalytique, comme l’ARN ribosomique. Des micro-ARN servent de matrice pour que des protéines appelées {facteurs puissent accomplir des fonctions catalytiques.
Les bases azotées qui constituent l’ARN sont l’adénine (A), la guanine (G), le cytosine (C) et l’uracile (U). La structure in vivo de l’ARN est conditionnée par la formation d’appariements internes entre bases complémentaires, A avec U, G avec C et, parfois, G avec U. La présence de cations divalents stabilise la structure, car ils bloquent les charges négatives des phosphates et empêchent ainsi leur répulsion électrostatique. L’ARN peut, comme l’ADN, présenter des structures secondaires et tertiaires.
Un simple brin peut, lorsque dans une région où des séquences inversées sont complémentaires, former localement une double hélice comme indiqué dans l’accroche (par exemple : -GUGCCACG—CGUGGCAC-).
D’un point de vue évolutif, on pense que l’ARN serait antérieur à l’ADN comme support de l’information génétique, ce qui expliquerait ses fonctions plus étendues et sa généralisation. L’ADN serait apparu plus tard et n’aurait supplanté l’ARN que pour le rôle de stockage à long terme, en raison de sa plus grande stabilité.
Si un brin d’ARN monocaténaire est endommagé, la lésion n’est pas réparée et le dommage est irréversible ; en revanche, si un des deux brins d’ADN est endommagé, la cellule peut utiliser l’information portée par le brin complémentaire intact pour réparer la lésion. La présence de thymine dans l’ADN permet à la cellule de détecter des lésions spontanées de la cytosine qui est sensible à l’oxydation. La désamination spontanée de la cytosine en présence d’oxygène convertit cette dernière en uracile. Grâce à la distinction thymine/uracile, la machinerie de réparation dite par excision de base (par les uracile-DNA glycosylases) peut détecter et corriger le défaut. Dans l’ARN, la désamination des cytosines produit des uraciles et n’est pas réparée. L’ARN a ainsi une durée de vie beaucoup plus courte que l’ADN : il est dégradé et recyclé. Cependant, pour la cellule, l’uracile est énergétiquement moins coûteux à produire que la thymine, car il nécessite une étape de synthèse de moins (méthylation par la thymidylate synthase).
La molécule d’uracile, découverte dès 1900, est très commune dans la nature, quoiqu’elle puisse être cancérigène et tératogène en cas d’exposition chronique ; elle semble aussi pouvoir être d’origine extraterrestre, selon les rapports isotopiques 12C/13C d’un composé organique trouvé dans le météorite Murchison ! Sa transformation biosynthétique fournit des bases (uridine) plus ou moins phosphorylées et glycosylées, assurant diverses fonctions dans les organismes vivants.
C’est en 1959 que la base pyrimidique halogénée 5-iodo-2′-désoxyuridine a été décrite comme marqueur de la prolifération cellulaire et donc vecteur potentiel de radioisotopes dans l’ADN. En effet, l’iode ayant le même rayon de van der Waals que le groupe méthyle de la thymine (respectivement 2.0 Å et 2.15 Å), la molécule iodée peut s’insérer dans l’ADN lors de sa synthèse ou de sa réparation. Le 5-fluoro-uracile est un anticancéreux, qui agit également comme un leurre (classe des anti-métabolites), sous forme de monophosphate de 5-fluorodésoxy-uracile, en bloquant l’activité de la thimidylate synthase.
Un autre 5-halogéno-uracile vient de faire une entrée remarquée sur la scène mondiale, le 5-chloro-uracile. Pour la première fois, une bactérie viable a été conçue dans laquelle une des bases naturelles de l’ADN a été remplacée par un composé synthétique ! Il s’agissait d’obliger Escherichia coli K12 (cf. E. coli), une espèce incapable de synthétiser la thymine nécessaire à son génome, et donc dépendante du milieu de culture, à évoluer vers des variants génétiques tolérant des concentrations de plus en plus élevées de 5-chloro-uracile toxique. Il a suffi d’environ 1 000 générations cellulaires pour que la quasi-totalité des bactéries ait remplacé la thymine de leur génome par le xénobiotique. En l’absence du xénobiotique, de tels organismes synthétiques ne peuvent évidemment pas survivre, et donc ne peuvent entrer en compétition ni échanger du matériel génétique avec les espèces sauvages. Après l’assemblage de morceaux d’ADN pour créer une bactérie synthétique comme Craig Venter, la machine qui reproduit la sélection naturelle et l’évolution pour Philippe Marlière ? Deux approches de la biologie synthétique…
Pensée du jour
« Après la révolution de la chimie par la synthèse au XIXe siècle, la révolution de la biologie par la synthèse au XXIe siècle ? »
Sources
– http://fr.wikipedia.org/wiki/Acide_ribonucléique
– http://en.wikipedia.org/wiki/Uracil
– http://en.wikipedia.org/wiki/Uracil-DNA_glycosylase
– http://fr.wikipedia.org/wiki/Fluorouracil
– http://en.wikipedia.org/wiki/Uracil-DNA_glycosylase
– www.cea.fr/le_cea/actualites/evolution_d_un_genome_bacterien-60034
– P. Marlière, J. Patrouix, V. Döring, P. Herdewijn, S. Tricot, S. Cruveiller, M. Bouzon, R. Mutzel: {Chemical Evolution of a Bacterium’s Genome, Angew. Chem. Int. Ed . 2011, 50(31), 7109-7114.
– http://fr.wikipedia.org/wiki/Biologie_synthétique

 Présentation
Présentation  Entités
Entités  Partenaires
Partenaires  Histoire de la SCF
Histoire de la SCF  Gouvernance
Gouvernance  Industrie
Industrie