Ce n’est qu’au début du XXe siècle que plusieurs laboratoires découvrent simultanément que les organes génitaux contiennent des substances ayant un intérêt thérapeutique. C’est en 1922 que l’hormone féminine est isolée : elle est nommée œstrogène, d’après œstrus, l’ensemble des phénomènes physiologiques liés à l’ovulation.
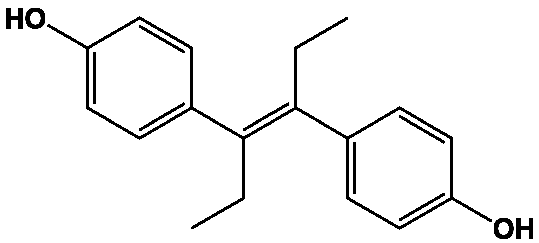
En 1938, un britannique, E.G. Dodds isole un œstrogène de synthèse, le diéthystilbestrol ou DES, le premier utilisable par voie orale et beaucoup plus puissant que l’œstrone elle-même.
Il en publie la structure dans la revue Nature cette même année, mais ne prend pas de brevet : à l’époque, les résultats de la Recherche universitaire, étaient librement publiés et offerts gracieusement à tous, scientifiques et industriels
Dès 1947, le DES, décrit comme un produit miracle (encore un !) permettant d’éviter fausses couches et accouchement prématurés, est commercialisé à travers le monde, et on lui ajoute quelques indications, comme combattre les complications de toute sorte de la grossesse, les effets négatifs de la ménopause, etc. Dix ans plus tard, la publicité en est encore faite comme médicament de la « la prophylaxie de routine dans toutes les grossesses ». Et pourtant !
En 1959, un décret interdit le DES aux Etats-Unis… dans la nourriture pour animaux uniquement, car son effet cancérigène sur les souris de laboratoire est décrit depuis quelques années. Il faudra attendre 1971 et les travaux du Dr Arthur Herbst, qui établit une relation sans équivoque entre l’apparition de cancers du vagin et du col de l’utérus dès l’adolescence et la prise, par leur mère, de DES pendant sa grossesse, pour que le DES soit interdit à la femme enceinte aux Etats-Unis. En 1977, il est interdit aux femmes enceintes en France, au Canada, en Allemagne, aux Pays-Bas et en Autriche ; l’Australie suit en 1978, l’Italie en 1981, la Hongrie en 1983…
En 1977 également, R.H. Kauffman publie la première description des anomalies utérines suspectées d’être liées à l’exposition au DES {in utero, et l’année suivante, Y. Brackbill met même en doute son action bénéfique dans les grossesses à risques. Il constate même que son utilisation provoque une augmentation significative du taux d’avortements spontanés tardifs, d’accouchements prématurés et de morts néonatales…
En France, Anne Cabau lance une des premières enquêtes sur le traitement par le diéthylstilbestrol et ses conséquences sur la reproduction par l’intermédiaire de la Mutuelle Générale de l’Education Nationale. Elle décrit les accidents pergravidiques qui sont plus fréquents chez les filles exposées au DES in utero et effectue la première publication française sur les anomalies utérines en 1982. En 1984, l’enquête du collège national des gynécologues-obstétriciens français portant sur 57 patientes dont l’exposition au diéthylstilbestrol est sûre, confirme les résultats publiés par A.L. Herbst en 1981. Stérilité, fausses couches précoces ou tardives, grossesses extra-utérines, cancers du sein sont les principaux risques encourus, mais on montre aussi que le DES agit sur le développement de l’utérus déjà formé, et est à l’origine de diverses déformations de l’utérus, des anomalies des trompes, etc. chez les « Filles DES ».
On peut très schématiquement retenir trois types d’action du DES sur les tissus cibles :
– Action carcinogène et mutagène sur le génome,
– Modifications enzymatiques probablement responsables d’anomalies fonctionnelles,
– Modifications de structure des épithéliums et des canaux de Müller et de Wolff.
« Mères DES » et « Filles DES » ne sont pas les seules à souffrir : les « Fils DES », exposés in utero, s’ils ne développent pas de cancers, présentent une plus grande fréquence de kystes bénins de l’épididyme, des hypotrophies des testicules, et diverses malformations de leur appareil génital.
Quant est-il de la génération suivante, la 3ème génération ? Des expériences menées sur les souris ont montré une fréquence accrue des cancers utérins, de kystes de l’ovaire chez les souris femelles, et une fréquence accrue des malformations génitales chez les souris mâles. Cette observation, évidemment non transposable à l’homme, a conduit à suivre attentivement la 3ème génération issue de « Mères DES ». Actuellement, avec un recul relativement important, les anomalies observées sont rares. Cependant, il n’est pas exclu que le risque d’une malformation grave de l’œsophage soit multiplié par 10 chez les « Petits-Enfants DES », le médicament pouvant alors être responsable d’effets extra-génitaux.
La Cour de Cassation, dans un arrêt du 24 septembre 2009, écrit « après avoir constaté que le DES avait bien été la cause directe de la pathologie tumorale… il appartenait alors à chacun des laboratoires pharmaceutiques de prouver que son produit n’était pas à l’origine du dommage ». La Cour d’Appel de Versailles a confirmé le 9 juin 2011 la responsabilité du médicament, pris par sa grand-mère, dans le lourd handicap (80 %) d’un jeune homme de 21 ans : le DES « a provoqué une malformation utérine chez sa fille qui, enceinte à son tour en 1989, a accouché d’un grand prématuré » pesant 1050 g.

Le Distilbène® est toujours commercialisé en France pour traiter le cancer de la prostate
Pensée du jour:
«Tout bon scientifique vit du et dans le doute ; toute thérapeutique et tout médicament le devraient aussi.»
Sources :
– http://fr.wikipedia.org/wiki/Diéthylstilbestrol
– http://en.wikipedia.org/wiki/Diethylstilbestrol
– E.G.Dodds, Estrogenic activity of certain synthetic compounds, {Nature 1938, 141, 247-249.
– R.H.Kaufman {et coll., Upper genital tract changes associated with exposure {in utero to diethylstilbestrol, {Am. J. Obstet. Gynecol. 1977, 128, 51-59.
– http://fr.wikipedia.org/wiki/Oœstrogène
– http://en.wikipedia.org/wiki/Estrogen
– http://d.e.s.chez-alice.fr/histoire.htm
– www.des-france.org/distilbene/consequences.php#miseaupoint
– Les Enfants du Distilbène, sous la direction de Bernard Blanc, Éditions Arnette, Paris, 1991
– http://afssaps-prd.afssaps.fr/php/ecodex/frames.php?specid=68600838&typedoc=R&ref=R0132579.htm

 Présentation
Présentation  Entités
Entités  Partenaires
Partenaires  Histoire de la SCF
Histoire de la SCF  Gouvernance
Gouvernance  Industrie
Industrie