Selon la nomenclature de l’IUPAC, les éthers sont désignés par le terme « alcoxyalcane », la chaîne alkyle la plus courte utilisant le préfixe alcoxy et l’autre chaîne, le suffixe alcane. Si l’éther fait partie d’une molécule plus complexe, il est décrit comme substituant alcoxy. Les règles de l’IUPAC ne sont pas toujours suivies pour les éthers simples, généralement parce que identifiés avant l’établissement des règles de nomenclature : éther éthylique ou diéthyl éther, anisole et phénétole (composants de l’arôme d’anis, cf. Arômes), vanilline (cf. Vanille et Vanilline), etc.
Pour les éthers cycliques, on utilise le nom qu’aurait un alcane cyclique ou l’atome de carbone est remplacé par un atome d’oxygène identifié par le préfixe {oxa : le tétrahydrofurane, ou THF, devrait ainsi s’appeler oxacyclopentane. Les polyéthers sont des composés avec plus d’une fonction éther. Le terme se rapporte généralement aux polymères qui contiennent ce groupe fonctionnel dans leur chaîne principale.
Contrairement à leurs précurseurs, les éthers ne peuvent pas former des liaisons hydrogène ce qui explique des points d’ébullition relativement à bas, comparés à ceux des alcools analogues. Cependant, la présence de deux paires d’électrons sur l’atome d’oxygène rend possible des liaison hydrogène avec des molécules d’eau : les éthers cycliques tels que le tétrahydrofurane et le dioxane-1,4 sont miscibles avec l’eau du fait de la plus grande exposition des atomes d’oxygène par rapport aux éthers aliphatiques.
Les éthers sont légèrement polaires, mais nettement moins que tous les autres composés oxygénés. Du fait de leur miscibilité avec beaucoup de produits organiques, ils sont souvent employés comme solvants. Ce sont des bases de Lewis et des bases de Brønsted. Ainsi, le diéthyléther forme un complexe avec le trifluorure de bore, l’éthérate BF3•OEt2 et coordonnent également le magnésium(II) des réactifs de Grignard (cf. Victor Grignard) ; mieux encore le tétrahydrofurane stabilisent les réactifs de Grignard vinyliques, ouvrant par cette découverte d’Henri Normant de nouvelles applications en synthèse organique. Les polyéthers, y compris beaucoup d’antibiotiques, des cryptands et des éthers couronne lient fortement les cations alcalins.
Les éthers, notamment le diéthyl éther et le tétrahydrofurane, forment facilement des peroxydes explosifs au contact de l’air, sous l’action de la lumière ou de la chaleur, nécessitant donc l’addition d’un antioxydant comme le BHT (2,6-bis(1,1-diméthyléthyl)-4-méthylphénol) pour les stabiliser.
L’essentiel du diéthyl éther est obtenu comme sous-produit de l’hydratation en phase vapeur de l’éthylène (cf. Éthylène) en vue de préparer l’éthanol (cf. Éthanol). Ce procédé emploie des catalyseurs supportés à base d’acide phosphorique (cf. Acide phosphorique) et peut être ajusté pour préparer plus d’éther si le besoin se fait sentir. La déshydratation en phase vapeur de l’éthanol au contact d’alumines acides peut donner des rendements de 95 % en diéthyl éther. Rappelons que la synthèse d’un additif antidétonant pour l’essence, le méthyl tert-butyl éther ou MTBE (cf. Méthyl tert-butyl éther) met également en jeu une catalyse acide entre le méthanol (cf. Méthanol) et l’isobutène. Le tétrahydrofurane est aussi obtenu par catalyse acide au départ du 1,4-butanediol :
mais cette réaction est actuellement supplantée par l’oxydation catalytique directe du butane (cf. Éthylène) en anhydride maléique qui est ensuite hydrogéné en THF, une réaction extraordinaire par sa sélectivité, puisqu’il y a incorporation dans l’intermédiaire maléique de trois atomes d’oxygène :
Une synthèse générale, employée à une moindre échelle est la synthèse de Williamson (1850), réaction de substitution nucléophile (S{N2) d’un halogénure d’alkyle ou d’aryle par un ion alcoolate.
Ce dernier est habituellement préparé immédiatement avant la réaction, ou formé {in situ. Dans les synthèses industrielles, la formation de l’alcoolate est généralement effectuée par catalyse de transfert de phase. L’acétonitrile ou le N, N-diméthylformamide sont les solvants généralement employés. Cette méthode est toutefois limitée aux halogénures d’alkyle primaires (et aux phénols) du fait de la réaction concurrente d’élimination pour les halogénures d’alkyle secondaires ou tertiaires. La synthèse de Williamson est couramment utilisée en synthèse organique multi-étapes pour la protection transitoire de fonctions alcool ou phénol.
Le diéthyl éther a été employé comme solvant de la nitrocellulose pour former, en association avec l’éthanol, le collodion, découvert par Louis Ménard en 1846. Il a servi à produire de nombreux types d’explosifs (cordite principalement, cf. Acide picrique), très résistants à l’humidité, à l’eau et à la biodégradation. C’est un fulminant qui -mis à feu- libère une grande quantité de gaz et de chaleur, presque sans fumée, et sans détoner brutalement. Il a donc été utilisé dans les douilles pour propulser les balles et obus avec un moindre danger de faire exploser le fut des fusils ou canons. En synthèse organique industrielle, le diéthyl éther est actuellement remplacé par d’autres éthers.
Mais la notoriété du diéthyl éther vient de son emploi en tant qu’anesthésique en Grande-Bretagne dès les années 1840 (cf. Chloroforme). Cependant ses effets secondaires très désagréables (nausées…) et sa toxicité, ainsi que le risque élevé de dépendance, ont fait qu’il n’est plus utilisé en France et dans de nombreux pays développés. Le diéthyl éther est parfois consommé comme substance psychoactive par inhalation des vapeurs : c’est l’éthéromanie, qui engendre des mouvements incontrôlés, des spasmes, une incapacité à parler intelligiblement. Une consommation régulière peut engendrer une dépendance physique et psychique forte.
Le THF est converti en présence d’acides forts en un polymère linéaire connu sous les noms de PTMO, (polytetramthylene oxide) ou PTMEG (poly(tetramethylene ether)glycol) qui est utilisé pour la fabrication de fibres élastomères de polyuréthane (cf. Polyuréthanes). C’est également un solvant employé en chimie des polymères, notamment du PVC (cf. PVC).
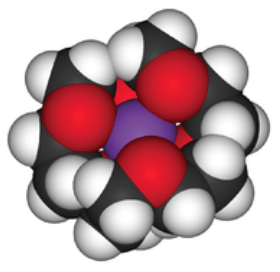
Le « dibenzo-18-couronne-6 » ou 1,4,7,10,13,16-hexaoxacyclooctadécane selon la nomenclature systématique de l’IUPAC, était né, démontrant la capacité de ces molécules à complexer des cations mono- et divalents et marquant une nouvelle ère dans la chimie, récompensée par le Prix Nobel de Chimie 1987, partagé avec Donald J. Cram et Jean-Marie Lehn, d’où la
Pensée du jour
« Même des éthers ont été couronnés par le Roi de Suède. »
Sources
– http://fr.wikipedia.org/wiki/Éther-oxyde
– www.faidherbe.org/site/cours/dupuis/ethe2.htm
– http://en.wikipedia.org/wiki/Ether
http://fr.wikipedia.org/wiki/Éther_diéthylique
– http://en.wikipedia.org/wiki/Diethyl_ether
– http://en.wikipedia.org/wiki/Ether
– http://en.wikipedia.org/wiki/Tetrahydrofuran
– http://fr.wikipedia.org/wiki/Collodion
– http://fr.wikipedia.org/wiki/Éther_couronne
– http://en.wikipedia.org/wiki/Crown_ether
– www.nobelprize.org/nobel_prizes/chemistry/laureates/1987/pedersen-lecture.html
Pour en savoir plus
– Jean-Baptiste Dumas
– Arômes
– Vanille et Vanilline
– Victor Grignard
– Éthylène
– Éthanol
– Acide phosphorique
– Méthyl tert-butyl éther
– Méthanol
– Acide picrique
– Chloroforme
– Polyuréthanes
– PVC

 Présentation
Présentation  Entités
Entités  Partenaires
Partenaires  Histoire de la SCF
Histoire de la SCF  Gouvernance
Gouvernance  Industrie
Industrie 

