C’est Claude Louis Berthollet qui découvrit ce nouveau sel de sodium en 1785, employé d’abord comme agent blanchissant des étoffes de coton qui jusqu’alors devaient être exposées au soleil sur de vertes prairies, puis comme agent bactéricide. Très vite populaire, la solution d’hypochlorite de sodium est produite de façon industrielle dans une petite usine située dans le quartier Javel à Paris qui commercialise alors la « liqueur de Javel ».
L’eau de Javel existe sous deux concentrations : normale à 2,6% en chlore en bouteille et concentrée à 9,6% en berlingot plastique. Si la préparation originale s’effectuait par barbotage de chlore dans une solution de soude selon la réaction :
Cl2 + 2 NaOH ——> NaOCl + NaCl + H2 O
le procédé Hooke emploie l’électrolyse d’une solution de chlorure de sodium qui engendre les deux réactifs mis en jeu. La consommation française était de l’ordre de 245 millions de litres en 2010.
Les propriétés de l’eau de Javel dépendent du chlore actif de la solution, c’est-à-dire des ions ClO– et Cl– dissous dans la solution. Aux propriétés d’oxydation utilisées pour le blanchiment et dans la composition de lessives, s’ajoutent des propriétés bactéricides dues à l’action de l’acide hypochloreux sur les bactéries. Avec le développement de l’hygiène au XIXème siècle, l’eau de Javel a certainement contribué à sauver des millions de vies humaines.
Elle est principalement utilisée pour assainir l’eau potable afin d’éviter la pollution bactérienne. En France la chloration limite à 0,2-0,3 mg/l la teneur en chlore alors qu’aux États-Unis, la limite est de 5 mg/l, l’odeur caractéristique étant l’indice d’une eau bien potable. Ne parlons pas des piscines !
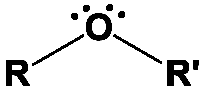
La cartouche ci-dessus décrit la structure ionique de l’hypochlorite de sodium qui est un produit très instable à l’état solide. L’anion hypochlorite ClO– est constitué d’un atome de chlore lié à un atome d’oxygène portant une la charge négative. La liaison s’effectue par la mise en commun de deux électrons, l’un provenant de l’atome de chlore, l’autre de l’atome d’oxygène. Il reste des doublets électroniques sur les atomes de chlore et d’oxygène, indiqués par les lobes bleus et orientés de manière spécifique dans l’espace. Pour satisfaire à la règle chimique de l’octet, un électron complémentaire doit être apporté à l’atome d’oxygène : il provient de l’atome de sodium qui se trouve donc sous sa forme ionisé de cation Na+.
La pensée du jour
Je préfère sentir l’eau de Javel plutôt que l’eau de Cologne, car c’est plus propre et en plus c’est français ! Attribuée à Georges Clémenceau en 1918
Sources
– http://fr.wikipedia.org/wiki/Eau_de_Javel
– www.lenntech.fr/procedes/desinfection/chimique/desinfection/desinfectants-hypochlorite-sodium.htm
– http://scienceamusante.net/wiki/index.php?title=Hypochlorite_de_sodium

 Présentation
Présentation  Entités
Entités  Partenaires
Partenaires  Histoire de la SCF
Histoire de la SCF  Gouvernance
Gouvernance  Industrie
Industrie