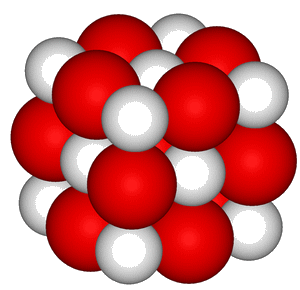
Le tétroxyde de plomb est un oxyde de plomb de masse molaire 685 qui se décompose vers 500°C. C’est un pigment artificiel connu depuis l’antiquité. Pline l’Ancien en rapporte son observation lors de l’incendie d’une villa. On le préparait à l’époque romaine en chauffant le blanc de plomb (carbonate de plomb ou céruse) dans des plats en le brassant à l’air jusqu’à ce qu’il change de couleur. Il était utilisé comme pigment imitant le cinabre qui est le sulfure de mercure, HgS. Au Moyen Age, on utilisait la céruse qu’on appelait aussi minium et qui est en vérité le carbonate de plomb PbCO3. Son usage s’est perpétué au XVI et XVIIèmes siècles comme poudre pour le visage, le cou et la gorge…
La faculté du minium de produire une couche protectrice sur les alliages ferreux et ses propriétés bactéricides et fongicides l’ont fait utiliser dans la construction, y compris pour le bois. Il était notamment utilisé comme revêtement du bois des bateaux pour éviter leur dégradation par les insectes et leur pourrissement. Dans les peintures murales et fresques, très utilisé jusqu’en 1930, il brunit avec le temps. Il a toutefois une meilleure tenue dans les tableaux peints à l’huile et tempera.
Les divers oxydes de plomb suivent les trois valences les plus usuelles du plomb :
– le monoxyde, PbO, ou litharge (Pb2+),
– le tétroxyde, Pb3O4, ou minium (Pb2+, Pb3+),
– le dioxyde PbO2, ou oxyde puce / scrutinyite (Pb4+).
Les oxydes de plomb sont présents dans les batteries au plomb mises au point en 1852 par Gaston Plantié et qui sont caractérisées par deux réactions électrochimiques :
– à l’anode :
Pb + HSO4– ———> PbSO4 + H+ + 2 e–
– à la cathode :
PbO2 + HSO4– + 3 H+ + 2 e– ———> PbSO4 + 2 H2O
Peu coûteuses, elles n’ont cependant qu’une capacité massique faible (35wh/K).
Du point de vue biologique, le minium, comme tous les sels de plomb, est très toxiques pour les cellules et ils engendrent le saturnisme notamment chez les jeunes enfants avec des troubles physiologiques et neurologiques. On a longtemps pensé que le déclin de la civilisation de Rome était du au réseau en plomb de l’adduction d’eau, en fait celle ci riche en carbonate de calcium amène un revêtement de carbonate sur les tuyaux qui empêche la dissolution de grandes quantités de plomb. Par contre, la vaisselle en plomb, très utilisée par les romains, ainsi que l’acétate de plomb, couramment ajoutée pour « sucrer » les vins, sont plus vraisemblablement à l’origine du saturnisme. En France la teneur maximum en plomb est fixée à 100μg/L de sang.
Les peintures au plomb sont interdites depuis 1948. Cependant, dans les immeubles anciens et peu ou mal entretenus, les poussières de peintures anciennes peuvent polluer l’atmosphère intérieure et entraîner des cas de saturnisme que l’on ne trouve plus maintenant que chez d’anciens mineurs ou ouvriers de la métallurgie du plomb. Pour diminuer globalement la teneur dans le sang des populations on a aussi progressivement supprimé le plomb tétraéthyle, Pb(C2H5)4, dans l’essence et carburants pour véhicules (cf. Platine).
Dans certaines populations du Moyen-Orient, d’Afrique ou d’Inde, les khôls à base de galène broyée (PbS) et de chlorures de plomb utilisés comme fards autour des yeux avec également des propriétés bactéricides, ont entraîné des cas de plombémies chez des enfants.
|Actuellement en France, les personnes les plus exposées sont les chasseurs et mangeurs de gibiers car il y a environ 8 000 à 9 000 t/an de grenailles de plomb dispersées dans la nature…
La pensée du jour
«À l’ouverture de la chasse, les risques d’être plombés ne sont pas seulement pour le gibier.»
Sources
– http://fr.wikipedia.org/wiki/Minium
– http://en.wikipedia.org/wiki/Lead(II)_oxide
– http://en.wikipedia.org/wiki/Minium_(mineral)
– http://en.wikipedia.org/wiki/Lead_dioxide
– http://fr.wikipedia.org/wiki/Batterie_au_plomb
– http://fr.wikipedia.org/wiki/Saturnisme
– http://fr.wikipedia.org/wiki/Khôl
– http://en.wikipedia.org/wiki/Kohl_(cosmetics)
Pour en savoir plus
– Platine

 Présentation
Présentation  Entités
Entités  Partenaires
Partenaires  Histoire de la SCF
Histoire de la SCF  Gouvernance
Gouvernance  Industrie
Industrie