Les neurostéroïdes, identifiés et nommés par Étienne-Émile Baulieu, le découvreur du RU 486 (cf. Stéroïdes et pilule) peuvent être soit produits dans le système nerveux à partir de stéroïdes circulants métabolisés sur place, soit des stéroïdes, dits neuroactifs, ayant un effet spécifique dans le cerveau ou les nerfs, et éventuellement être produits localement.
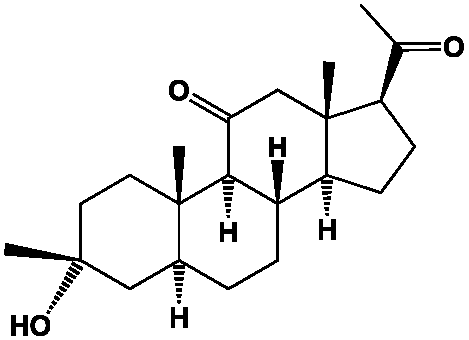
Ainsi, la progestérone (PROG), la prégnénolone (PREG) et la déhydroépiandrostérone (DHEA) sont produits dans le cerveau mais également apportés par la circulation sanguine à partir des glandes surrénales.
Le métabolisme cérébral de la PROG conduit à une série de composés réduits qui agissent comme modulateurs allostériques des récepteurs des neurotransmetteurs de type GABAA (cf. GABA). Par exemple, la 3α-hydroxy-5α-pregnan-20-one augmente l’importation d’ions chlorures associée au fonctionnement du GABAA, alors que les sulfates de PREG et de DHEA ont l’effet inverse ! Le premier est une molécule effectrice positive qui joue le rôle d’agoniste, les seconds le rôle d’antagoniste des récepteurs, avec des changements de conformation qui se propagent d’un site à un autre du récepteur. Dans le cas des canaux ioniques, il y aura donc modulation du signal électrique au niveau synaptique et variation de l’excitabilité du neurone.
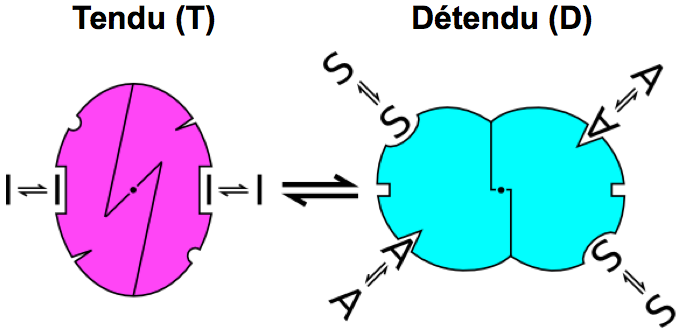
L’allostérie (du grec ἄλλoς, allos : autre et στερεός, stereós : solide) est un mode de régulation de l’activité d’une protéine, notamment d’une enzyme, par lequel la fixation d’une molécule, dite effectrice, modifie les conditions de fixation d’une autre molécule, en un site distant de cette protéine.
Le développement, dans les années 1965, du modèle de transition concertée pour les protéines allostériques dit de Monod-Wyman-Changeux (Jacques Monod est Prix Nobel de physiologie et de médecine 1965) est toujours un cadre conceptuel majeur en biologie.
Il explique les propriétés coopératives de protéines régulatrices comme l’hémoglobine (cf. Hémoglobine), pourquoi et dans quelles conditions elle libère le dioxygène (cf. Dioxygène).
La transition allostérique d’une protéine entre des états D et T est régulée par des conditions extérieures changeantes : substrats et agonistes stabilisent la forme D, alors qu’un inhibiteur stabilise la forme T. Ce mécanisme, qui agit un peu comme un interrupteur dans un circuit électrique, est très souvent rencontré dans les voies métaboliques : plus le produit final s’accumule, plus la réaction initiale est lente, et moins de produit est formé. Ce phénomène régule la production d’une substance qui peut être toxique en grande quantité, et constitue un modèle de contrôle énergétique !
D’autres fonctions pharmacologiques des neurostéroïdes, par exemple l’activité anesthésique de l’alfaxalone par modulation du transport d’ions chlorure au niveau de la membrane cellulaire du neurone, mise en évidence en 1987. En 1994, on s’est aperçu que le site de liaison aux récepteurs GABAA de l’alfaxalone, comme celui d’autres neurostéroïdes comme l’alfadolone, l’hydroxydione et le minaxolone utilisés en anesthésie générale, était différent de celui des benzodiazines, comme on l’avait cru initialement.
L’épilepsie répond bien à l’administration de ganaxolone, un neurostéroïde anticonvulsant, analogue de l’allopregnanolone naturelle, qui présente en outre des propriétés sédatives et anti-anxiolytiques. Des antidépresseurs comme la fluoxétine et la fluovoxamine (cf. Prozac), qui agissent comme inhibiteurs sélectifs de la recapture de la sérotonine, conduisent à une augmentation significative du taux de certains neurostéroïdes.
Cet effet expliquerait même, selon certains auteurs, l’action du Prozac® ! Des études expérimentales chez le rongeur révèlent l’action bénéfique des neurostéroïdes sur la performance mnésique de l’animal ainsi que leurs effets neuroprotecteurs contre la cytotoxicité induite par les acides aminés excitateurs et les peptides β-amyloïdes (formant des plaques dites séniles). Chez l’humain, les données, bien qu’encore parcellaires, montrent l’existence de corrélations significatives, dans des échantillons de régions cérébrales de patients âgés atteints de la maladie d’Alzheimer, entre les faibles concentrations en divers neurostéroïdes d’une part et d’autre part les taux élevés de protéines β-amyloïdes et l’hyperphosphorylation de la protéine Tau. La protéine Tau, dont la croissance anarchique en «buissons » affecte le fonctionnement des cellules du cerveau, est un marqueur du développement de la maladie d’Alzheimer et d’autres affections neurodégénératives.
Quant au DHEA, également associé en France au nom de Baulieu, il a été largement médiatisé à partir de 1996 sous le nom d’hormone de longue vie. Plus de 2 000 publications décrivent ses bienfaits au niveau neurologique et immunitaire, dans les situations de stress, comme modulateur hormonal et dans de très nombreux dysfonctionnements liés à l’âge (son taux diminue rapidement, et jusqu’à -70 %, à partir de 70 ans). Quasi-miraculeux, une pilule quotidienne dosée à 50 mg, administrée pendant 6 mois à des personnes âgées, restaurerait leur taux de DHEA au niveau de celui d’un adolescent ! Mais attention, rajeunir n’est pas sans danger a fini par penser le Docteur Faust !
Le DHEA est un des neurostéroïdes observés en réponse à la maladie d’Altzheimer, à l’administration d’antidépresseurs, etc. Il aurait aussi une action sur l’IGF (Insulin Growth Factor), en relation avec l’activité de l’insuline et l’accumulation de graisse, et donc une action favorable sur l’athérosclérose et les maladies cardiaques. Il serait également recommandé dans le traitement de cancers non hormonaux dépendants, limitant la prolifération cellulaire, au moins dans des modèles animaux comme les rongeurs. Par contre, des doses élevées de DHEA sans supplémentation en antioxydants, causent, toujours chez les rongeurs, des dégâts hépatiques sévères. D’autres contre-indications sont répertoriées : problèmes de prostate, problèmes hépatiques, etc.
Pensée du jour
« Bien loin du modèle simpliste « clé-serrure », le vivant et sa régulation, c’est si compliqué et si délicat à ajuster, qu’il vaut mieux éviter de le perturber ! »
Sources
– E.E. Baulieu, Neurosteroids: {A New Regulatory Function in the Nervous System. Humana Press, 1999, ISBN 0-89603-545-X
– www.ncbi.nlm.nih.gov/pmc/articles/PMC3139029
– http://fr.wikipedia.org/wiki/Allosterie
– http://en.wikipedia.org/wiki/Allosteric_regulation
– http://fr.wikipedia.org/wiki/Jean-Pierre_Changeux
– http://cat.inist.fr/?aModele=afficheN&cpsidt=17466677
– http://en.wikipedia.org/wiki/Ganaxolone
– www.jle.com/e-docs/00/04/50/25/article.md?fichier=images.htm
– http://fr.wikipedia.org/wiki/Maladie_d’Alzheimer
– www.institut-baulieu.org/actualites/vers-nouvelle-méthode-traitement-maladie-d’alzheimer
– http://fr.wikipedia.org/wiki/Déhydroépiandrostérone
– www.lifeextensionvitamins.com/dhea.html
Pour en savoir plus
– Cholestérol
– Testostérone
– Stéroïdes et pilule
– GABA
– Hémoglobine
– Dioxygène
– Prozac

 Présentation
Présentation  Entités
Entités  Partenaires
Partenaires  Histoire de la SCF
Histoire de la SCF  Gouvernance
Gouvernance  Industrie
Industrie