Les PBDE (polybromodiphényléthers) ont été largement utilisés dans de nombreux produits plastiques et textiles, dans les applications électriques et électrotechniques, dans les produits de construction et dans les mousses polyuréthanes. Composés organiques, ils sont facilement introduits dans les matrices thermoplastiques et thermodurcissables. Les plus courants sont les dérivés penta-, octo- et déca-bromés. Les polybromobiphényles (PBB) et l’hexabromocyclododécane (HBCD) obtenu à partir du cyclododécatriène (cf. Butadiène) possèdent des propriétés similaires.
Efficaces certes, mais dangereux : leur faible tension de vapeur les rend volatils au point de contaminer des sites éloignés (on en trouve dans l’air de la région des Grands Lacs et dans le Grand Nord, dans les boues du lac Michigan, et généralement à des teneurs élevées en Amérique du Nord, au Québec…). A haute température, ils dégagent des fumées toxiques. Ils sont liposolubles, c’est dire qu’ils s’accumulent dans les chaînes trophiques, d’autant qu’ils sont peu biodégradables (demi-vie de 2 ans et plus). Plus de 82 % du déca-PBDE utilisé dans le monde auraient été absorbés par les organismes vivants, notamment aquatiques, en Amérique du Nord : carpes, dauphins, phoques et belugas du Saint-Laurent, goéland argenté, mais aussi en mer du Nord : hareng atlantique, merlan et morue. Amphibiens et oiseaux ne sont pas épargnés, non plus que les animaux piscivores.
La toxicité des PBDE semble multiple : système endocrinien, hépato-toxicité, hyperplasie thyroïdienne (par similitude avec la structure de la thyroxine), neuro-toxicité (comportement moteur, développement cognitif), cancérogénicité… En conséquence, la législation s’est durcie jusqu’à interdire ces composés dans de très nombreux pays (sauf dans des cas particuliers, contrôlés) : 2004, renforcé en 2005 en Europe, 2006 et 2008 au Canada, 2012 au niveau fédéral aux États-Unis où déjà 10 États les ont interdits.
Cette interdiction d’usage s’accompagne maintenant d’une surveillance des niveaux d’exposition et de contamination des produits alimentaires. En France, une étude (EAT2, juin 2011) sur les contaminants chimiques dans l’alimentation montre que le risque sanitaire est bien maîtrisé pour la population générale. Huit congénères de PBDE ont bien été détectés dans 76 % des 4 600 analyses effectuées, mais à des taux 12 à 15 fois inférieurs à ceux détectés avant l’interdiction. Quant aux niveaux d’exposition, le relargage de PBDE lors de la destruction ou du recyclage des innombrables produits en contenant demandera un suivi sur encore plusieurs années, de même que des études toxicologiques approfondies.
Devons-nous alors choisir entre le risque sanitaire et le risque incendie ? Certainement pas, car le chimiste et la chimie ne manquent pas de ressources ! Même si l’approche a longtemps été et reste encore très pragmatique. Les recherches s’orientent vers les matériaux peu ou pas fumigènes (pour limiter les émanations toxiques), vers les systèmes intumescents (qui gonflent sous l’action de la chaleur pour former une mousse microporeuse isolante appelée « meringue »), et vers la prise en compte de la fin de vie des structures ignifugées… Le gouvernement allemand a, dès 2001, lancé un très important programme sur ce sujet, avec un examen exhaustif des divers composés utilisés et utilisables, leur mode d’action (parfois mal défini) et la toxicité des produits et des dérivés de combustion.
Les qualités des retardateurs, outre un maximum d’innocuité sur l’environnement, peuvent être de différentes natures. Ils peuvent soit
-** abaisser la température lorsque leur dégradation est endothermique. C’est le cas des hydroxydes d’aluminium et de magnésium, et de plusieurs hydrates minéraux. Ils sont par exemple utilisés dans les polyoléfines pour câbles,
– constituer un bouclier thermique, isolant les zones encore épargnées. Ce sont les additifs dits intumescents,
– diluer l’air ambiant en produisant un gaz inerte comme le dioxyde de carbone ou de la vapeur d’eau ;
– piéger les radicaux hautement réactifs, H• et OH•, présents dans la flamme, par la formation de radicaux X•, de moindre énergie et limitant donc sa propagation…
Ce sont souvent des mélanges complexes qui sont utilisés, afin d’assurer la conjugaison de plusieurs de ces propriétés. Ils sont utilisés soit en phase condensée, soit en phase vapeur.
Les hydroxydes métalliques, comme l’hydroxyde d’aluminium ou ATH (cf. Aluminium), sont efficaces à des taux de charge élevés (40 à 50 %) dans des résines thermodurcissables (polyesters…). Ils sont donc employés dans des matériaux de gros tonnage, comme les résines utilisées notamment dans les aménagements des transports en commun (trains, etc.). Des additifs, comme des silanes, des acides gras, sont ajoutés pour optimiser la rhéologie des mélanges, ainsi, parfois, que des borates de zinc pour améliorer la cohésion du résidu d’alumine en cas de feu. L’addition d’agents dits de synergie, oxydes de bore, de zinc, aluminosilicates (zéolithes, argiles), permet de stabiliser les intermédiaires de combustion et renforce la cohésion du goudron, mais limite le gonflement du bouclier carboné.
Les dérivés du phosphore (cf. Phosphore, Acide phosphorique) sont particulièrement appréciés. Certains, comme les phosphates, sont utilisés de longue date. D’abord mis en œuvre dans les peintures, car polaires, ils n’étaient utilisés que dans des phases aqueuses. Associés dans des charges complexes carbonées, ils peuvent s’intégrer dans des polymères thermoplastiques et thermodurcissables et leurs propriétés en tant que retardateurs en sont renforcées. Les phosphates minéraux, pyrophosphates et surtout polyphosphate d’ammonium (APP), sont très appréciés : intégrés dans des systèmes complexes, ils jouent le rôle de sources acides (à chaud, ils forment de l’acide phosphorique et de l’ammoniac), réagissant sur des précurseurs carbonés pour conduire finalement à un bouclier phosphocarboné. Avec un agent gonflant, on obtient un « meringuage » efficace. En présence de composés cellulosiques (cf. Cellulose), ils dégagent du dioxyde de carbone (cf. Dioxyde de carbone) qui dilue l’oxygène de l’air ambiant et ralentit la combustion.
Les phosphates organiques comme le bis(diphénylphosphate) de résorcinol, à l’origine de goudrons peu combustibles, sont utilisés dans les polymères techniques PC/ABS, PVC-bâtiment. Le phosphinate d’aluminium, plus stable thermiquement que les homologues phosphatés, est un candidat intéressant pour l’avenir, lequel semble devoir se jouer autour des différents degrés d’oxydation du phosphore substitué ou non par des groupements azotés.
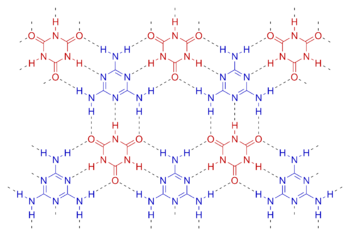
Le cyanurate de mélamine, (C3H6N6-C3H3N3O3), est en fait un sel stabilisé par liaisons hydrogène, utilisé pour sa stabilité à haute température (300 °C), malgré sa toxicité : il forme une structure bi-dimensionnelle en réseau, proche de celle du graphite (cf. Carbone).
Le trioxyde d’antimoine (cf. Antimoine) est également un retardateur réputé, malgré sa toxicité topique, et utilisé dans les appareillages électriques, les textiles, le cuir et divers revêtements, généralement en association avec des composés halogénés. Les goudrons formés sont particulièrement peu inflammables.
Pensée du jour
« Déclarer sa flamme sans mettre le feu aux poudres, là est l’honneur du chimiste. »
Sources
– http://fr.wikipedia.org/wiki/Grand_incendie_de_Londres
– http://fr.wikipedia.org/wiki/Incendies_de_Kyoto
– http://fr.wikipedia.org/wiki/Polybromodiphényléther
– http://www.chemicalsubstanceschimiques.gc.ca/fact-fait/pbde-fra.php
– S. Posner, L. Börås, {Aperçu et évaluation technique des solutions de rechange à l’éther de Decabromodiphenyl (DecaBDE) en plastiques. Stockholm : Produits chimiques suédois, inspection, juin 2005
– www.hc-sc.gc.ca/hl-vs/iyh-vsv/environ/pbde-fra.php
– http://www.anses.fr/Documents/PASER2006sa0361Ra2.pdf
– www.gtfi.org/doctech/retardateur_de_flamme.pdf
– www.oekorecherche.de/english/berichte/volltext/FSM-cont.pdf
– http://en.wikipedia.org/wiki/Ammonium_polyphosphate
– www.nissanchem-usa.com/melamine-cyanurate.php
– http://en.wikipedia.org/wiki/Antimony_trioxide
– A. Leisewitz, et al. : {Substitution ambiante des retardements appropriés de flamme, Principes fondamentaux d’évaluation, Résultats et vue d’ensemble (résumé). Berlin, Allemagne : Agence environnementale fédérale (Umweltbundesamt), juin 2001.
– http://en.wikipedia.org/wiki/Flame_Retardant
Pour en savoir plus
– Butadiène
– Aluminium
– Phosphore
– Acide phosphorique
– Cellulose
– Dioxyde de carbone
– Carbone
– Antimoine

 Présentation
Présentation  Entités
Entités  Partenaires
Partenaires  Histoire de la SCF
Histoire de la SCF  Gouvernance
Gouvernance  Industrie
Industrie